Získávání kovů z rud na principu redoxních reakcí
Většina kovů se vyskytuje v přírodě ve formě sloučenin. tyto sloučeniny se nazývají minerály (nerosty). Minerály ze kterých můžeme kovy získat se nazývají rudy. Z těch se kovy získávají pomocí různých technologií. Jedny z nich využívají redoxních reakcí (vyredukování kovů z jejich oxidů).
| Většina kovů se vyskytuje v přírodě ve formě sloučenin – minerály (nerosty).
Minerály ze kterých můžeme kovy získat se nazývají rudy.
Jednou z metod získávání kovů je vyredukování kovů z jejich oxidů (využití redoxních reakcí). |
Výroba železa



- minerály ze kterých se železo získává jsou většinou oxidy (magnetit Fe3O4, hematit Fe2O3, limonit Fe2O3.nH2O)
- pokud se kovy vyskytují ve formě sulfidů (např. ZnS) musí se převádět na oxidy
2 ZnS + 3 O2 → 2 ZnO + 2SO2
2 ZnO + C → 2 Zn + CO2
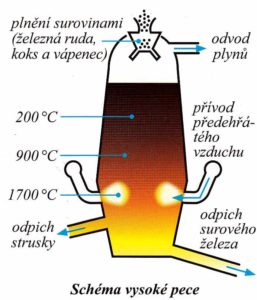
- výroba železa probíhá ve vysoké peci
- do vysoké pece se zavážejí železná ruda, koks, vápenec a vhání se sem vzduch
- suroviny se nejprve vysuší a poté se postupně ruda redukuje na železo
- vysoká pec pracuje řadu let
- plní se nepřetržitě surovinami
- zhruba každé 2 hodiny dochází k odpichu (vypouštění) železa a strusky
- surové železo obsahuje 3-4% uhlíku
- dále se zpracovává na litinu (více než 1,7% C) a ocel (méně než 1,7% C)
probíhají tyto reakce:
- spalováním koksu se pec vyhřívá na 1700 – 2000°C, vzniklý CO2 se redukuje na CO, dochází k roztavení rudy a vzniku tekuté strusky
C + O2 → CO2
CO2 + C → 2 CO,
- redukce oxidem uhelnatým (ve vyšších vrstvách pece)
3 Fe2CO3 + CO → 2 Fe3O4 + CO2
Fe3O4 + CO → 3 FeO + CO2
FeO + CO → Fe + CO2
- redukce uhlíkem (ve spodní části pece)
Fe2O3 + 3 C → 2 Fe + 3 CO
Kovy se mohou vyrábět také z kovových odpadů. Výroba je méně náročná, spotřebuje se méně energie a je šetrnější k životnímu prostředí.
| Výroba železa
minerály
Ve vysoké peci probíhají tyto reakce:
C + O2 → CO2 CO2 + C → 2 CO
3 Fe2O3 + CO → 2 Fe3O4 + CO2 Fe3O4 + CO → 3 FeO + CO2 FeO + CO → Fe + CO2
Fe2O3 + 3 C → 2 Fe + 3 CO |
Na co umět odpovědět:
|
CITACE: viz. odkaz: [k. 1 – chemie], [k. 2 – chemie]
obrázek (magnetit – Vzorek magnetitu z italského regionu Trentino-Alto Adige.): Autor: Archaeodontosaurus – Vlastní dílo, CC BY-SA 3.0, https://commons.wikimedia.org/w/index.php?curid=11052142
obrázek (hematit – mineral. Nikon E-8800): Autor: Luis Miguel Bugallo Sánchez (Lmbuga Commons)(Lmbuga Galipedia)Publicada por/Publish by: Luis Miguel Bugallo Sánchez – Vlastní dílo, CC BY-SA 3.0, https://commons.wikimedia.org/w/index.php?curid=340268
obrázek (limonit – Vzorek limonitu): Autor: Luis Miguel Bugallo Sánchez (Lmbuga Commons)(Lmbuga Galipedia)Publicada por/Publish by: Luis Miguel Bugallo Sánchez – Vlastní dílo, CC BY-SA 3.0, https://commons.wikimedia.org/w/index.php?curid=340262
